来源:科学大院
《我不是药神》中的 “神药”格列宁,从费城染色体的发现、到发现酪氨酸激酶抑制剂能够杀灭异常的粒细胞到FDA加速批准上市,它的诞生之路足足走了41年。
为什么新药的发明需要那么长的时间?传统中药变身现代药物中间要跨越哪些难关?今天,大院就跟你说说中国科学院上海药物研究所花费13年研制“丹参多酚酸盐”,又在上市后的13年中不断深入研究的故事。

图1 丹参多酚酸盐研究团队获得第一个奖励——中国科学院先进集体(2017)(图片来源:宣利江供)
发现了它 丹参有望脱胎换骨
今天故事的主角,它的前身是著名的中药——丹参。从2000多年前的《神农本草经》开始,历代本草均有记载。丹参及其制剂,被广泛应用于心脑血管疾病的治疗。

图2丹参(Salvia miltiorrhiza),唇形科鼠尾草属植物丹参的根和根茎(图片来源:丹参植物:植物网,丹参生药材:宣利江供)
长期的民间应用和临床实践说明,丹参这种植物确实具有心脑血管的保护作用,但是,用现代医药的观点来看,丹参的应用面临重重问题:
首先是成分不明。想象一下,来源于植物的中药材通过煎煮会得到一大碗棕色的“汤药”,其中可能有数十甚至上百种化学成分,丹参中究竟是什么物质在保护心脑血管?

图3。中药(图片来源:视觉中国)
成分不明确使得丹参及其制剂的质量不可控,疗效和安全性无法保证。以丹参注射液为例,国内曾经有上百家企业生产,每个企业的产品质量标准不统一,更为糟糕的是质量标准不严格,并不能反应疗效和安全性,这给临床用药安全带来了很大的隐患。
此外,没有经过现代药理药效和毒理学研究认可和GCP规范下的临床研究,仅仅基于经验来说明一个药品的疗效和安全性已不符合现代循证医学、精准医学的要求。
丹参如何在被人类使用2000年后完成打怪升级,再一次脱胎换骨?第一步,就是要找到丹参药材中的有效成分。
传统丹参制剂如丹参注射剂是以水溶性成分为主要的化学成分,于是上海药物所的科学家团队特别关注和研究了丹参的水溶性成分。1992年,他们发现丹参中的多酚酸类成分都是以盐的形式存在于生药材中,包含镁盐、钾盐、铵盐等。药理活性筛选结果显示不同成分的体内外药理作用是不同的,其中丹参乙酸镁是心脑血管保护活性最强的化合物,它在药材中含量高达3%~5%,这在天然产物中是很罕见且非常难得的。
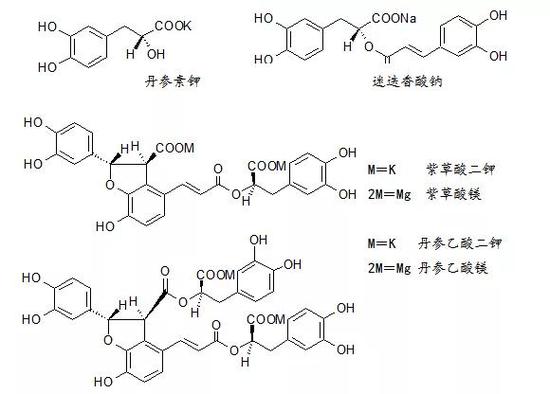
图4。 丹参中主要的水溶性有效成分
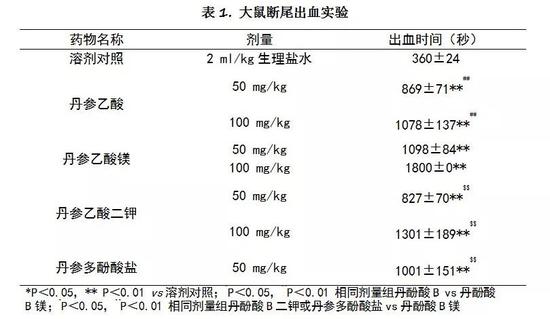
这个发现至关重要,说明前人对丹参药理作用的物质基础的认识是不足的,尤其是忽略了丹参乙酸镁这个关键成分。基于此,他们提出了以丹参乙酸镁为质量标准的核心来开展丹参新制剂的研究的创新设想,研究目标终于锁定了,他们开始走上了长达十三年的新药研发之路。
新药研发路上 pk三大问题
在丹参多酚酸盐整个研发过程中,上海药物所的科研人员大胆尝试了别人不敢尝试的,作为中药制剂,实现了很多的“国内第一”:
第一次以丹参乙酸镁作为丹参注射剂质量控制核心;
第一次用近100%的有效成分研制中药注射剂;
第一个中药采用运动平板试验评价临床疗效;
第一次中药开展多成分的动物药代动力学试验;
第一次中药开展了多成分的人体药代动力学试验;
第一次药品上市后大规模的Ⅳ期临床试验;
第一个中药开展了3万例的真实世界疗效和安全性研究……
新药研发显然不可能一蹴而就,从丹参到丹参多酚酸盐,科学家面临的棘手问题很多,最核心的还是质量、疗效和安全性这三大要素。
成分明确&质量可控:严格与权衡
质量是新药的源头,质涉及的是明确的成分,量涉及的是可控性。
成分明确需要严格的质量标准和质量的全程控制来保证。药品的质量标准中涉及鉴别、检查、含量测定等几十项控制项,每一个控制项的设立需要基于对药品的质量研究,药品法规的要求,高标准和可行性的权衡。
对于一个药品来说,质量的结果是分析得到的,但这个结果的实现需要质量的设计、工艺步骤和质量过程控制来保证。比如注射剂要求是无菌的,经过了提取分离和精制过程得到的丹参多酚酸盐原料药一般可以通过无菌检测,但是生产过程中仍需要经过一道无菌处理。
角度不一样,要求也不一样。从合格产品角度,每一批次药品的合格出厂需要通过每一个质量标准项,一票否决。但从生产角度,又需要保证生产出来每一批次产品都能符合质量标准,高标准和高合格率是一对矛盾,需要权衡。新药研发的过程就是一个权衡的过程,早期的阶段更多的是疗效和安全性的权衡,大生产时是高标准和可行性的权衡,所有的权衡都需要研究数据的支撑。
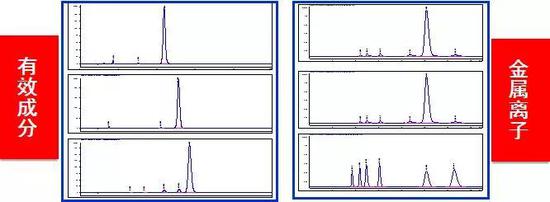
图5。丹参多酚酸盐的有效成分和金属离子指纹图谱
药品中的成分明确可控了是不是代表药品成分明确了呢?并不是,还要研究药品进入人体后会发生什么变化。药品对人体会产生药效作用,人体反过来又会对药品产生代谢作用,不仅要了解代谢产物是什么,还需要了解它们的浓度。达不到有效浓度,就谈不上疗效,反过来超过了最低的安全性的限度,药效就变成了毒性,这就是药品的双刃剑特征。
多成分的药代动力学研究发现,丹参多酚酸盐类成分具有口服生物利用度差,代谢速度快、单次和多次甲基化后从胆汁排泄、在心脏、肝脏、肾脏具有较高的分布浓度的代谢特征。这样,丹参多酚酸盐的体内过程就清晰了,同时也说明了静脉滴注是丹参多酚酸盐的一个合理给药方式,有利于在2小时的滴注期保持稳定的血药浓度来发挥药效。
从实验室到工业化生产,是一个不断放大的过程。大多数新药研发人员对工业化生产是没有具体经验的,实验室小试技术有时候在工业化大生产时并不可行。对科研人员来说这是一个不断学习、自我否定和提高的过程。举一个简单的例子,在实验室给样品换一个容器可能只是一个随手下意识的动作,但工业化生产时就会多出一条管道、两个储罐以及配套的阀门、电机等,还要考虑设备的布局、走向,使用时还涉及具体的技术参数和论证、清洗流程等等。一个非常简单的环节会增加设备和人员成本、能耗、生产时间,还会增加产品质量的风险因素。
上海药物所的研究人员克服了重重困难:没有条件,研究人员自己去尝试创造,没有制药工业化方面的知识背景和经验,就去反复查文献,向制药专业人士请教,最终他们自主设计建造了一条工业化的生产线。虽然现在看来是非常粗糙的,但就是在这条生产线上完成了丹参多酚酸盐的“中试放大”,甚至最初的规模化生产。

图6。 丹参多酚酸盐原料药和制剂生产线一角(图片来源:宣利江供)
药物会产生什么作用,通过什么机制来实现?
我们要去一个地方,可以乘坐汽车、飞机甚至步行,每一种方法都有各自的利弊。新药的研发也是如此,时刻在进行权衡评价,找到疗效和安全性的平衡点。
丹参多酚酸盐可以保护心血管系统的结果相对容易得到证实,但是具体机制是怎样的?
上海药物所的科研团队通过大量的药理药效研究发现丹参多酚酸盐具有通过钙离子通道拮抗扩张血管、通过抗血小板聚集、抗凝血来抑制血栓形成、通过抗氧化、抗炎来保护内皮细胞和缺氧复氧损伤等多种疗效特征,在每一条途径上我们都可以找到一个代表性的化学药,而丹参多酚酸盐的疗效是每条途径药理作用的综合体现,这种药理作用特征恰好对心脏微循环障碍具有很好的改善作用,而这恰恰是心血管疾病领域没有被满足的临床需求。
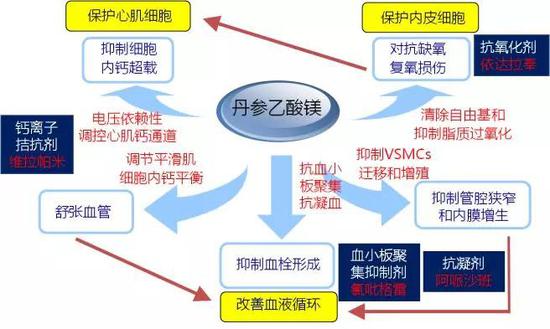
图7。丹参多酚酸盐通过多种机制和途径保护心血管系统的作用特征
然后,这些药效特征通过随机、双盲、对照、多中心的临床研究得到了验证,对冠心病心绞痛患者,丹参多酚酸盐在心绞痛发作次数、硝酸甘油用量、心电图疗效等指标上疗效显著,并作为首个中药通过了黄金标准——运动平板试验的验证,丹参多酚酸盐可以显著提高患者的运动级别和运动当量。其显著的疗效在大规模的临床应用中也得到了良好体现。
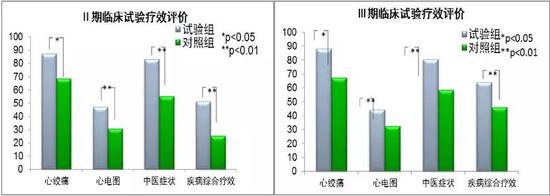
图8。 丹参多酚酸盐的II、III期临床研究疗效
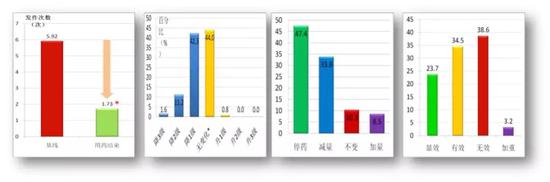
图9。 丹参多酚酸盐IV期临床疗效
安全性更需要关注
安全性问题有的和药品中有效成分相关,有的与药品的杂质成分相关,有的是和药物的临床使用方式相关(比如药物药物的相互作用引起的不良反应)。所以,安全性的保证同样涉及一个药物的整个流程,需要尽可能地排除或者降低各种安全性风险。
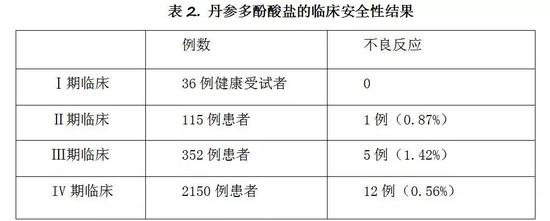
安全性指标同样要经过动物试验、人体临床的研究来验证。相对于疗效,安全性问题是小概率事件,因此,涉及安全性隐患的发现更为困难,很多药物的安全性问题是在药品上市后才得以发现,比如万分之一概率的不良反应是不可能在几百或者几千的临床研究病例中发现的。这就是近年来国内外针对药品安全性关注越来越严并贯穿药品从研发到临床应用整个生命周期的重要原因之一。
幸运的是,丹参多酚酸盐从研发到迄今为止2000万以上病患使用过程中在安全性上表现不错,实现了安全的目标,当然这还不够,在安全性问题上,没有最好,只有更好。
结语
迄今,丹参多酚酸盐走过了十三年的新药研发、十三年的临床应用之路,从1992年发现主要活性成分开始,2005年获新药证书和生产批文,2009年被列入《国家医保目录》,获国家技术发明二等奖,已在全国5000多家医院临床应用,2000多万患者受益,这条路还在不断延续。丹参多酚酸盐为实现中药现代化提供了借鉴范例,入选了中国科学院改革开放40年40项标志性重大科技成果。